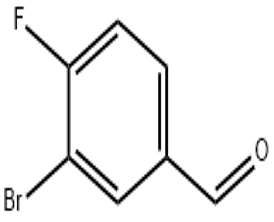
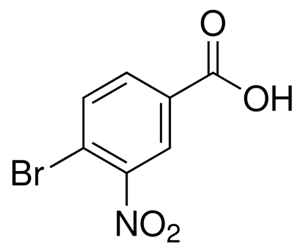
alfa-ionon (CAS#127-41-3)
| Kodovi rizika | R42/43 – Može izazvati preosjetljivost udisanjem i kontaktom s kožom. |
| Sigurnosni opis | S24/25 – Izbegavati kontakt sa kožom i očima. |
| WGK Njemačka | 2 |
| RTECS | EN0525000 |
| TSCA | Da |
| HS kod | 29142300 |
alfa-ionon(CAS#127-41-3) informacije
Ljubičasti keton, takođe poznat kao benzofenon, je organsko jedinjenje. Evo nekoliko sigurnosnih informacija o iononeu:
1. Toksičnost: Ljubičasti keton ima određenu toksičnost za ljudsko tijelo. Može izazvati oštećenje centralnog nervnog sistema i jetre i može imati štetne efekte na reproduktivni sistem i embrione.
2. Opasnost od udisanja: Udisanje pare ili prašine jonona može izazvati simptome nelagodnosti kao što su vrtoglavica, pospanost, kašalj i otežano disanje. Dugotrajno izlaganje može uzrokovati oštećenje centralnog nervnog sistema.
3. Opasnost od kontakta: Ljubičasti keton se može apsorbirati kroz kožu. Dugotrajan ili opsežan kontakt može izazvati iritaciju kože i očiju. Pri rukovanju jononom treba nositi odgovarajuću ličnu zaštitnu opremu kao što su rukavice i zaštitne naočare.
4. Mjere za gašenje požara: U slučaju curenja ili požara, za gašenje požara koristiti suvi prah, pjenu ili ugljični dioksid. Izbjegavajte korištenje vode, jer ljubičasti keton reagira s vodom i proizvodi zapaljive plinove.
5. Odlaganje otpada: Odložite otpadni ljubičasti keton na odgovarajući način u skladu sa lokalnim propisima i pravilima. Nemojte ga ispuštati u kanalizaciju ili kantu za smeće.
6. Mere opreza pri skladištenju: Ljubičasti keton treba čuvati na hladnom, suvom, dobro provetrenom mestu, dalje od izvora vatre i oksidanata.
Ove informacije su samo za referencu. Ako je potrebna dalja upotreba ili obrada jonona, pogledajte relevantni sigurnosni list i konsultujte stručnjaka.
priroda
Ljubičasti keton, takođe poznat kao linailketon, je prirodno jedinjenje ketona. To je glavna komponenta arome cvijeća ljubičice.
Ljubičasti keton je bezbojna do blijedo žuta uljasta tečnost koja je isparljiva na sobnoj temperaturi.
Ljubičasti keton je rastvorljiv u alkoholu i eterskim rastvaračima, a slabo rastvorljiv u vodi. Gustina mu je relativno mala, sa gustinom od 0,87 g/cm³. Osetljiv je na svetlost i može da apsorbuje ultraljubičaste zrake.
Ljubičasti keton može se oksidirati u ketonske alkohole ili kiseline u kemijskim reakcijama, a može se reducirati u alkohole reakcijama redukcije hidrogenacije. Može se podvrgnuti reakcijama alkilacije i esterifikacije s mnogim spojevima.
Metoda primjene i sinteze
Ljubičasti keton (također poznat kao ljubičasti keton) je aromatično jedinjenje ketona. Ima poseban miris i često se koristi u industriji parfema i parfema. Slijedi uvod u upotrebu i metode sinteze jonona:
svrha:
Parfemi i začini: karakteristike mirisa jonona, koji se široko koristi u industriji parfema i začina za proizvodnju mirisnih proizvoda ljubičice.
Metoda sinteze:
Sinteza jonona se generalno postiže pomoću sljedeće dvije metode:
Oksidacija nukleobenzena: Nukleobenzen (benzenski prsten sa metilnim supstituentom) je podvrgnut reakciji oksidacije, kao što je upotreba oksidirajuće kiseline ili kiselog rastvora kalijum permanganata, da bi se dobio jonon.
Spajanje pirilbenzaldehida: pirilbenzaldehid (kao što je benzaldehid sa supstituentima piridinskog prstena u para ili meta položaju) reaguje sa anhidridom sirćetne kiseline i drugim reaktantima pod alkalnim uslovima da bi se formirao jonon.